Archives de catégorie : Non classé
Explorer le dysfonctionnement cognitif chez les patients atteints de COVID long : anomalies des mouvements oculaires et implications des circuits frontaux-sous-corticaux via l’oculométrie et l’apprentissage automatique
Dépistage des troubles visuels
Une étude exhaustive menée par l’INSERM en 2002, commandée par la Mutuelle Générale de l’Éducation Nationale (MGEN), jette une lumière nouvelle sur l’importance cruciale du dépistage précoce et de la prise en charge des troubles visuels dès le plus jeune âge.
Avec une analyse basée sur près de 1 500 documents scientifiques, ce rapport souligne que plus de 10% des enfants de moins de 5 ans en France pourraient souffrir d’un ou plusieurs déficits visuels, impactant potentiellement leur développement global et leurs capacités d’apprentissage.
Les déficits les plus communs, tels que l’hypermétropie, la myopie, l’astigmatisme, et le strabisme, peuvent, sans diagnostic et traitement précoces, conduire à une baisse irréversible de l’acuité visuelle. Cette recherche soulève donc l’importance d’une évaluation systématique et précoce pour prévenir les conséquences à long terme sur la qualité de vie et l’intégration sociale des enfants affectés.
Ce rapport met également en lumière les avancées dans les méthodes de dépistage et les options de traitement, encourageant une approche multidisciplinaire pour un impact significatif sur la santé publique.
Pour les professionnels de la santé, les éducateurs et les parents, cette étude représente une ressource précieuse pour mieux comprendre et agir contre les déficits visuels dès le plus jeune âge.
#SantéVisuelle #DépistagePrécoce #INSERM #MGEN #SantéPublique #Pédiatrie
VIDÉO : Le monde à travers les yeux d’une personne déficiente visuelle cérébrale
Comment le regard social se développe-t-il chez l’enfant autiste?
17 au 23 septembre partout en France : Semaine De L’Equilibre & Du Vertige
Faire du bruit partout en France
La semaine de l’Équilibre et du Vertige 2023 se tiendra partout en France du 17 au 23 Septembre afin de se synchroniser avec les différents pays qui participent à l’évènement. Notre communauté dans sa pluralité va être invitée à « faire du bruit » sur tout le territoire Français, en écho à la « Balance Awareness Week » organisée au niveau mondial, la même semaine, par la Vestibular Disorders Association Américaine (VEDA)
Affiche de la semaine:
Toutes les informations sur https://gdrvertige.com/semaine-de-lequilibre-du-vertige/
Des données référencées:
Fiche épidémiologique désordres vestibulaires (données colligées sur 10
ans ; GDR Vertige 2023)
• En France, les vertiges représentent le 3e motif de consultation chez le généraliste après les fièvres et
les maux de tête, avant les maux d’estomac et les douleurs lombaires » (Goslan. Medecine & Science
N°805 Mars 2014)
• Le vertige et les instabilités représentent # 4% des symptômes principaux dans le département des
urgences hospitalières. Les vertiges d’origine vestibulaire représentent annuellement à eux seuls 1% de
toutes les urgences hospitalières (Rising Annual Costs of Dizziness Presentations to U.S. Emergency
Departments. Ali S. Saber Tehrani, MD, Diarmuid Coughlan, MPharm, MSc, Yu Hsiang Hsieh, PhD, MS,
Georgios Mantokoudis, MD, Fredrick K. Korley, MD, Kevin A. Kerber, MD, MS, Kevin D. Frick, PhD, and
David E. Newman-Toker. ACADEMIC EMERGENCY MEDICINE 2013; 20:689–696)
• Le coût total annuel relatif aux patients arrivant avec une plainte pour vertiges dans les services
d’urgence aux USA est estimé à plus de 4 milliards de $ par an (environ 4 % du coût total de l’ensemble
des urgences). Les vertiges d’origine vestibulaire représentent donc 1 milliard de $ pour les services
d’urgence aux USA (Tehrani AS, Coughlan D, Hsieh YH, Mantokoudis G, Korley FK, Kerber KA, Frick KD,
Newman-Toker DE. Rising annual costs of dizziness presentations to U.S. emergency departments. Acad
Emerg Med. 2013 Jul;20(7):689-96. doi: 10.1111/acem.12168. PMID: 23859582.)
• À partir de l’âge de 60 ans, environ 30 % de la population aura présenté les symptômes des désordres
vestibulaires à un moment de la vie (Brosel S, Strupp M. The Vestibular System and Ageing. Subcell
Biochem. 2019; 91:195-225. doi: 10.1007/978-981-13-3681-2_8.) Annuellement les désordres
vestibulaires représente 5% de toutes les prescriptions médicales des plus de 50 ans (Hulse et al. 2018:
Peripheral Vestibular Disorders: An Epidemiologic Survey in 70 Million Individuals. Hülse R, Biesdorf A,
Hörmann K, Stuck B, Erhart M, Hülse M, Wenzel A. Otol Neurotol. 2019 Jan;40(1):88-95. doi:
10.1097/MAO.0000000000002013.)
• En soins primaires, jusqu’à 10 % de tous les adultes consultent un médecin en raison de vertiges
(Corrales CE, Bhattacharyya N (2016) Dizziness and death: an imbalance in mortality. The Laryngoscope
126:2134–2136 https://doi.org/10.1002/lary.25902 ; Rieger A, Mansmann U, Maier W et al (2014)
Management of patients with the cardinal symptom dizziness or vertigo. Gesundheitswesen 76:e32–
e38. https://doi.org/10.1055/s-0033-1357145.)
af
• L’hypofonction vestibulaire uni- ou bilatérale altère l’équilibre et la mobilité et peut conduire à des
blessures ou à une invalidité dues à des chutes. L’ampleur de ce problème dans la population générale
est encore inconnue et très probablement sous-estimée. L’hypofonction vestibulaire pourrait affecter
entre 53 et 95 millions d’adultes en Europe et aux États-Unis. Bien que toutes les personnes affectées
ne ressentent pas l’ensemble des symptômes et leurs conséquences, des mesures diagnostiques et
thérapeutiques adéquates devraient devenir la norme de soins pour réduire le poids social de la maladie.
(Grill E, Heuberger M2,4, Strobl R1,2, Saglam M2
, Holle R5
, Linkohr B6
, Ladwig KH6,7, Peters A6
, Schneider
E8
, Jahn K2
, Lehnen N2,7. Front Neurol. 2018 Dec 7;9:1076. doi: 10.3389/fneur.2018.01076. eCollection
2018.)
• Des coûts annuels estimés entre 10 à 20 milliards de dollars sont associés aux blessures liées aux chutes
qui constituent la 6e cause de décès chez les personnes âgées, avec un taux de mortalité de 20 %. Avec
une augmentation estimée à 115 % de la population gériatrique de plus de 65 ans d’ici 2050, le nombre
de patients souffrant de troubles de l’équilibre et d’un système vestibulaire déficitaire atteindra
certainement des proportions quasi épidémiques. (Zalewski, C. 2015. Aging of the Human Vestibular
System. Seminars in Hearing, 36(03), 175–196.doi:10.1055/s-0035-1555120.)
Measurement of fusional vergence: a systematic review
1ère journée nationale sur les troubles neurovisuels
1ère journée nationale sur les troubles neurovisuels
16 Juin 2023 (9h00-18h00)
Salle des fêtes, Mairie du XVIème, 71 av. Henri Martin, Paris
1ère journée nationale sur les troubles neurovisuels programme definitif
Contact et inscription par mail : sophie@lesyeuxdanslatete.org
09h00 Accueil des participants
09h15 Ouverture, Accueil de Madame Scarlett Spziner, Conseillère
Régionale, Présidente de la Commission pour la Permanence
artistique et culturelle, Ile de France
09h30 Allocution de Madame Claire Compagnon
Déléguée Interministérielle à l’Autisme et aux troubles du
Neurodéveloppement
09h45-10h15 Troubles neurovisuels et troubles du neuro-développement :
quels liens ? Sylvie Chokron (INCC, Paris)
10h15-10h45 Prématurité et troubles sensori-moteurs : Retour sur la cohorte
EPIPAGE 2. Pr Stéphane Marret (Service de Néonatalogie,
Rouen)
10h45-11h15 Pause
11h15-11h45 Vision, Troubles du Spectre Autistique et troubles neuro-
développementaux : de l’expérimentation à la recherche
participative, Marie Pieron (INCC, Paris)
11h45-12h15 Influence des processus d’apprentissage moteur sur l’attention
visuo-spatiale des enfants atteints de paralysie cérébrale
unilatérale. Pr Yannick Bleyenheuft, Institute of Neuroscience,
UCLouvain
12h15-12h45 Table Ronde : Place des troubles neurovisuels dans les troubles
du neurodéveloppement (Pr Elie Saliba, Tours ; Pr S. Marret,
Rouen, Pr Catherine Barthélémy, Tours, Dr Paul Olivier, Paris, Dr
Cendra Aghulon, Paris, Dr T. Butel, Paris, Paris, Dr Sylvie
Chokron, Paris). Modération : Dr Céline Perez.
12h45-14h00 Déjeuner
14h00-14h30 Sensori-motricité et développement précoce de l’enfant.
Dr Christine Assaiante (LNC, Marseille)
14h30-15h00 Dépistage systématique des troubles neurovisuels en PMI:
l’exemple de l’Essonne et du Val d’Oise (Dr Camille Barthe,
Juvisy, Dr Claire Favrot, Paris).
15h00-15h30 L’ophtalmologiste face aux troubles neurovisuels (Dr Laurent
Laloum, Paris)
15h30-15h50 Pause
15h50-16h10 Dépistage et prise en charge des troubles neurovisuels en
orthoptie (M-L Laborie, Montauban) (présentation filmée)
16h10-16h30 La place de l’orthophoniste dans la prise en charge des troubles
neurovisuels. Marie Baduel (Orthophoniste, Paris)
16h30-16h50 La place de l’ergothérapeute dans la prise en charge des
troubles neurovisuels. Claire Mouchard Garelli (Ergothérapeute,
Lyon)
16h50-17h10 La place de la psychomotricité dans la prise en charge des
troubles neurovisuels. Sophie Allard (Psychomotricienne, Paris)
17h10-17h30 « Ils ont appris à voir » : Témoignages d’enfants porteurs de
troubles neurovisuels et de leurs familles
17h30-18h00 Vers la création d’un réseau national de prise en charge des
troubles neurovisuels : VISION-R (INCC & Association Les Yeux
dans la tête).
18h00 : Fin de la journée.
[WEBINAIRE N°12 DE LA SFERO] Couleurs, Perception Visuelle et Oculomotricité – mes expériences avec les filtres IRLEN
« Couleurs, Perception Visuelle et Oculomotricité – mes expériences avec les filtres IRLEN »

BILLETERIE A VENIR
VOEUX 2023

La SFERO vous souhaite le meilleur pour cette nouvelle année 2023.
Nous avons été heureux de vous proposer tout au long de l’année 2022 des rencontres scientifiques riches et passionnantes, poursuivons l’aventure ensemble en 2023.
Belle année à tous
L’équipe de la SFERO
[WEBINAIRE N°9] Base du contrôle neuronal du mouvement des yeux
[REPORTAGE ARTE]L’oeil et la vision: Les avancées scientifiques
[PUBMED] Troubles des mouvements oculaires dans les troubles du mouvement
Troubles des mouvements oculaires dans les troubles du mouvement
- PMID : 35402641
- PMCID : PMC8974874
- DOI : 10.1002/mdc3.13413
Abstrait
Le bilan oculomoteur est un élément essentiel de l’examen clinique neurologique et est particulièrement important lors de l’évaluation des patients présentant des troubles du mouvement. La majeure partie du cerveau est impliquée dans le contrôle oculomoteur, et donc de nombreuses affections neurologiques présentent des anomalies oculomotrices. Chacune des différentes classes de mouvements oculaires et leurs caractéristiques peuvent fournir des informations importantes qui peuvent faciliter le diagnostic différentiel. Cette revue pédagogique présente une approche clinique des anomalies des mouvements oculaires couramment observées dans le parkinsonisme, l’ataxie, la dystonie, la myoclonie, les tremblements et la chorée. Dans le parkinsonisme, des signes subtils tels que des secousses carrées proéminentes, un nystagmus optocinétique vertical altéré et/ou le « tour des maisons » signe suggérant une paralysie supranucléaire progressive précoce du regard avant que le regard vertical ne soit limité. Dans l’ataxie, le nystagmus est courant, mais d’autres signes tels que l’apraxie oculomotrice, la paralysie du regard supranucléaire, une fixation altérée ou la poursuite saccadique peuvent contribuer à des diagnostics tels que l’ataxie avec apraxie oculomotrice, Niemann-Pick de type C ou l’ataxie télangiectasie. Les myoclonies d’Opsoclonus et les myoclonies oculo-palatines présentent une phénoménologie caractéristique et sont généralement faciles à identifier. L’examen oculomoteur est généralement sans particularité dans les dystonies isolées, mais la crise oculogyre est une urgence médicale et doit être reconnue et traitée rapidement. L’impersistance du regard chez un patient atteint de chorée suggère la maladie de Huntington, mais chez un patient souffrant de dystonie ou de tremblement, la maladie de Wilson est plus probable. Pour terminer,
Mots-clés : œil ; troubles du mouvement; oculomoteur; poursuite; saccadés.
© 2022 Société internationale des troubles de la maladie de Parkinson et du mouvement.
Comment les innovations thérapeutiques peuvent modifier votre prise en charge des patients DMLA
Première cause de malvoyance dans les pays industrialisés après l’âge de 50 ans, la DMLA présente une fréquence de 3% entre 70 et 80 ans et de 12% après 80 ans. Cette maladie touche environ 1,5 million de personnes en France. On estime que le nombre de cas devrait augmenter de 50% d’ici 20 ans. Dans sa forme « humide » (exsudative), elle peut être traitée efficacement depuis la révolution des anti-VEGF dans le milieu des années 2010. Pour la DMLA « sèche » (atrophique), la plus fréquente, les espoirs reposent sur les dernières stratégies thérapeutiques (prothèse rétinienne, thérapie optogénétique…).
Restaurer la vision par stimulation des cellules rétiniennes
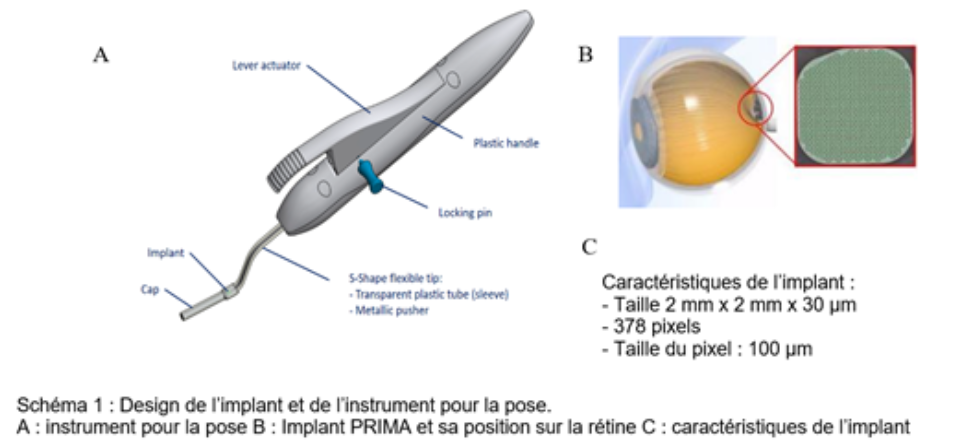
- Implant rétinien Prima. Développé par Pixium Vision, l’entreprise créée dans le cadre de l’Institut de la vision en 2011, cet implant sous rétinien s’adresse aux patients atteints de DMLA atrophique (DMLA sèche, sans néo-vascularisation). Le système Prima repose sur une « prothèse » sans fil, de 2mm sur 2 mm, implanté sur la rétine, qui s’apparente à une plaque de photorécepteurs électroniques sensibles à l’infrarouge. Une fois l’implant positionné, le patient porte des lunettes munies d’une caméra : celle-ci capte les images visuelles qui sont converties en images infrarouges pour générer une perception visuelle centrale artificielle.
« Une première étude Prima (sur 5 patients) a montré la faisabilité du système, la facilité et l’innocuité de l’implantation », a souligné Serge Picaud, chercheur à l’Institut de la vision, qui a présenté les différentes stratégies thérapeutiques à l’étude, lors du colloque Basse Vision d’Optic 2000. « Elle a validé une amélioration de l’acuité visuelle chez des patients, qui ont pu atteindre entre 20/460 et 20/565 (seuil de cécité 20/200 aux États-Unis), et la possibilité de combiner la vision centrale prosthétique, générée par le système Prima, et la vision périphérique naturelle qui reste au patient ». Une seconde étude Primavera, en cours auprès de 38 patients, doit confirmer ces résultats. C’est la dernière étape clinique avant la demande d’autorisation de mise sur le marché européen pour le traitement de la DMLA sèche.
- Thérapie optogénique. Alternative aux prothèses rétiniennes, la thérapie optogénique fait également l’objet d’une étude clinique, lancée par l’entreprise Gensight Biologics, au sein du service du professeur Sahel aux Quinze-Vingts. Son principe ? Introduire (en une seule injection) dans les cellules rétiniennes un gène d’algue qui « code » la protéine opsine afin de les rendre sensibles à la lumière. Cette thérapie nécessite elle aussi que le patient soit équipé de lunettes dotées de caméra pour augmenter l’intensité lumineuse des images (uniquement en noir et blanc). Après une expérimentation sur le primate, un essai clinique est en cours sur un patient atteint de rétinopathie pigmentaire.
- Thérapie sonogénétique. Dernière solution thérapeutique à l’étude chez les rongeurs : la thérapie sonogénétique. Elle consiste à produire des images ultrasonores pour une restauration visuelle au niveau cortical.
Quelles évolutions dans la prise en charge orthoptique et par l’opticien ?
Ces nouvelles approches thérapeutiques qui visent à restaurer la vision centrale chez les patients vont modifier de fait leur rééducation orthoptique. « Contrairement à une rééducation basse vision « classique », le but de la rééducation dite prosthétique est de permettre au patient de percevoir le signal dans sa zone d’atrophie maculaire là où est situé l’implant », a expliqué lors du colloque Basse Vision Serge Sancho, orthoptiste aux Quinze-Vingts, qui prend en charge les patients avec implants sous-rétiniens.
« Les premiers résultats de rééducation orthoptique chez les patients avec implant rétinien sont ‘’bluffants’’ »
La rééducation commence par un réglage des « lunettes » munies de caméra, une fois la réfraction faite : ajustement des plaquettes, des contrepoids sur les branches, de la hauteur de la caméra et de la teinte des verres. Ceci pour obtenir le meilleur signal pour le patient et pour que le laser soit directement en face de l’implant. « Dans un premier temps, le patient doit bien comprendre quand l’implant est stimulé et apprendre à regarder de nouveau en face », a précisé Serge Sancho. Cela nécessite un travail oculomoteur et, si besoin, sur micropérimètre. « C’est une rééducation longue et difficile qui peut être chronophage pour certains patients » a-t-il conclu. Avec à la clé, une majorité de patients avec des résultats « bluffants » : identification de motifs, de chiffres et de lettres.
Que la prise en charge soit « classique » ou avec implant, le rôle de l’opticien, spécialiste de basse vision, se révèle décisif pour optimiser les capacités visuelles restantes ou restaurées dans le but de procurer au patient la plus grande autonomie possible. Demain, pour les patients avec implants, son rôle pourrait bien s’étendre à l’accompagnement du patient dans la bonne gestion des « lunettes » avec caméra.
Myopie chez les adolescents et les adultes : les nouveaux résultats de la première grande étude épidémiologique française née du partenariat entre KRYS GROUP et le CHU de Poitiers sont publiés
Les Echos : Dix innovations pour améliorer sa vue
100 activités génériques de pédagogie active – Fiches complètes
https://fr.cursus.edu/22407/100-activites-generiques-de-pedagogie-active-fiches-completes-gratuit
Radiothérapie et phosphènes
Spot de sensibilisation de l’UNAPEI , pour une société plus inclusive
Actualités de l’INSERM : Une quantité de sommeil adaptée dès le plus jeune âge protègerait la vision
À partir de données de la cohorte EDEN, destinée à connaître les déterminants de la santé chez l’enfant, une équipe parisienne montre qu’une durée de sommeil nocturne trop faible ou trop importante à l’âge de deux ans est associée à un risque accru de porter des lunettes à l’âge de cinq ans. Elle établit ainsi un lien précoce entre sommeil et vision.


